导语:近日,首都医科大学刘怡教授团队与BEBC游民黎副教授团队合作,首次开发出具有显著抗炎特性的Poly-T序列修饰的金纳米棒(PTM AuNRs),通过抑制M1型巨噬细胞极化,激活巨噬细胞AMPK通路,抑制巨噬细胞炎症水平,成功缓解牙周炎症及骨破坏,为免疫调控疗法开辟新路径。
研究背景及内容
牙周炎是全球第二大口腔疾病,影响全球超10亿人,不仅导致牙齿脱落,还与糖尿病、心血管疾病等全身性疾病密切相关。牙周炎过度活化的免疫反应是疾病进展的关键推手——M1型巨噬细胞释放大量促炎因子(如TNF-α、IL-1β、IL-6等),引发“炎症风暴”,破坏牙龈胶原纤维并激活破骨细胞,最终导致牙槽骨吸收。传统疗法聚焦抗菌,难以调控过度免疫反应,因而效果有限,患者常面临复发难题。
为此。研究团队设计了一种Poly-T序列修饰的金纳米棒(PTM AuNRs)。以高生物相容性的金纳米棒为内核,表面修饰非免疫原性的Poly-T单链DNA,形成稳定的“核酸外衣”;通过抑制M1型巨噬细胞分化,降低促炎因子TNF-α、IL-6、IL-1β的分泌,同时激活AMPK通路,重塑细胞代谢平衡;纳米棒可被巨噬细胞高效摄取,并在细胞内长时间驻留,实现长效抗炎。通过检测脂多糖诱导的炎症环境中,巨噬细胞M1标志物和促炎因子的表达,检测PTM AuNRs的体外抗炎效果。通过蛋白质组学揭示PTM AuNRs抗炎的相关机制。通过在结扎诱导的小鼠牙周炎模型中,局部注射PTM AuNRs后,观察牙周组织巨噬细胞分化情况、炎症水平及骨吸收水平,检测PTM AuNRs的体内抗炎效果。通过检测牙周组织相关信号通路的活化情况,验证蛋白质组学的机制分析结果。该研究首次将核酸修饰纳米材料的免疫调控特性与金纳米棒的递送优势结合,突破了传统疗法‘重杀菌、轻调控’的局限。可通过局部注射实现‘炎症微环境重塑’,为牙周炎提供了一种新型治疗策略,也为其他慢性炎症性疾病的治疗提供理论基础及技术支撑。
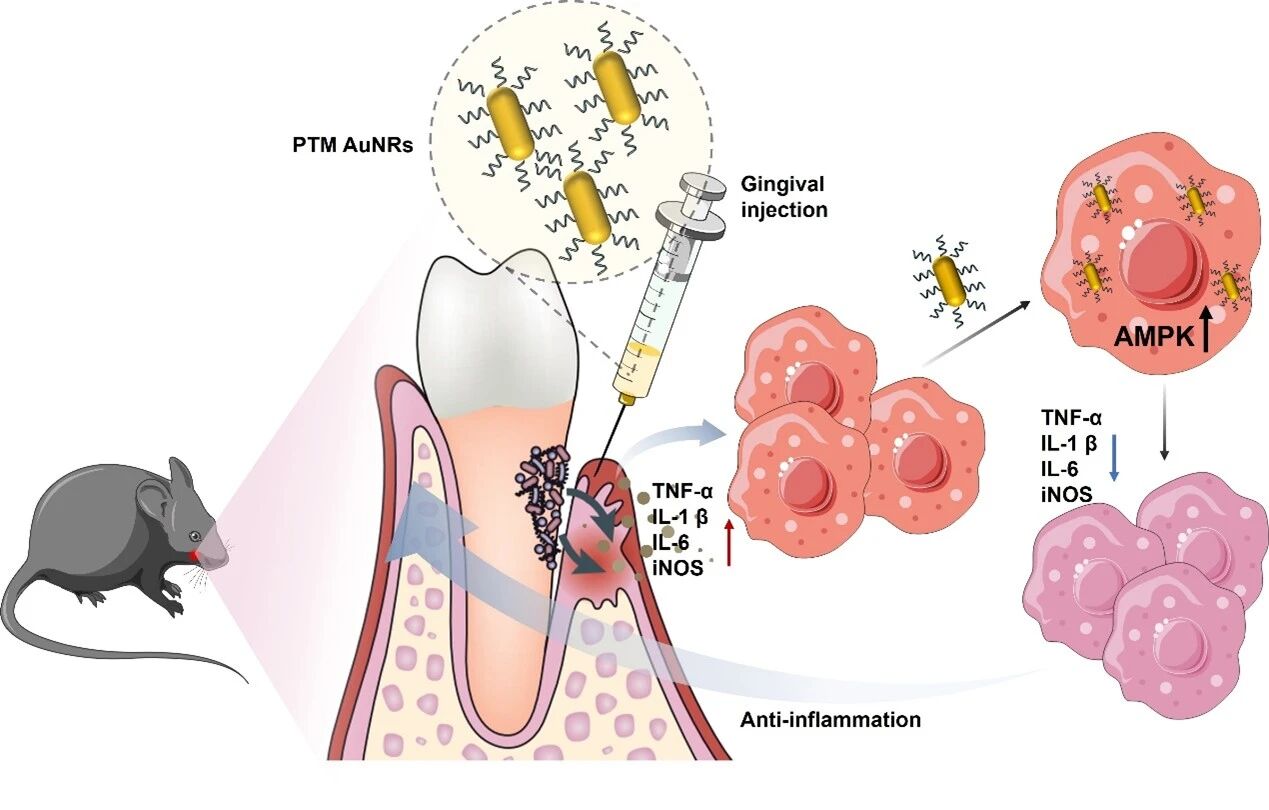
图1 PTM AuNRs 治疗牙周炎的治疗机制示意图
该研究成果以“Poly-T-Modified Gold Nanorods Suppress Macrophage-Mediated Inflammation for Periodontitis Therapy”为题,发表在国际材料科学期刊《ACS Applied Materials & Interfaces》上。
论文链接:https://doi.org/10.1021/acsami.5c00470
BEBC理念
西安交通大学仿生工程与生物力学研究所(BEBC)围绕“重大疾病诊治”领域中共性科学问题和技术挑战,按照“临床重大需求牵引-生物力学理论创新-医工核心技术突破-临床转化应用推广”的研究思路,创立了“多尺度生物热-力-电耦合学”,开拓了“力-医学”学科新方向,提出了“细胞智能”颠覆性概念和技术。BEBC立足力学基础理论,交叉融合材料、化学、生物、医学等领域,按照“临床问题(BED)-实验室研究(BENCH)-临床应用(BED)”的研究思路,在力学微环境领域开展了从组织到细胞和分子尺度的多尺度生物热-力-电耦合学等基础和应用研究,为阐明重大疾病的发病机理和临床诊疗提供有效的理论指导和技术方案。
近年来,BEBC在生物力学和力学生物学的研究基础上,通过工程学手段,将不同尺度的力学调控引入疾病诊疗,开展了一系列的“力医学(mechanomedicine)”研究,同时正在结合数据科学与人工智能将智能算法融入临床医学,积极开拓基于AI赋能的“数智力医学”研究领域。相关代表性研究成果发表于《自然材料》(Nature Materials)、《自然化学》(Nature Chemistry)、《自然生物医学工程》(Nature Biomedical Engineering)、《自然通讯》(Nature Communications)、《科学进展》(Science Advances)、《美国科学院院报》(PNAS)等期刊。在国内医学权威期刊上系统阐释了力医学在不同疾病中的应用及前景。