近年来,纳米技术与微纳驱动系统的快速发展为高灵敏度生物检测提供了新思路。西安交通大学仿生工程与生物力学研究所(BEBC)谢磊研究员和徐峰教授在Analytical Chemistry发表“Selective Interfacial Assembled Asymmetric Porous Nanomotors as Maneuverable Labels for Boosting Capture and Ultrasensitive Detection”的研究性文章,该研究提出了一种基于选择性界面组装策略制备的智能非对称多孔纳米马达,实现了在光热驱动下的自主运动与多信号放大检测,为生物传感与癌症早筛提供了创新方案。
研究内容简介
癌症早期诊断对提高治愈率至关重要,但传统免疫传感器在低浓度分析物检测中灵敏度不足。针对这一挑战,团队创新性地将自驱动纳米马达引入免疫传感体系,通过构建具备磁性、光热性、孔结构和催化活性的非对称纳米马达,实现了高效抗原捕获与信号放大。该团队以乳腺癌标志物CA153为模型,通过红外光照诱导纳米马达产生热泳运动,显著提高了抗体标记与抗原分子的碰撞概率,捕获效率相比静态标签提升95.8%。研究中,团队利用选择性界面自组装技术实现了Fe₃O₄、介孔二氧化硅、聚多巴胺及铂纳米酶的多组分精确空间分布,构建了具有多通道信号输出(比色、光热及催化)的双介孔非对称纳米结构(图1)。
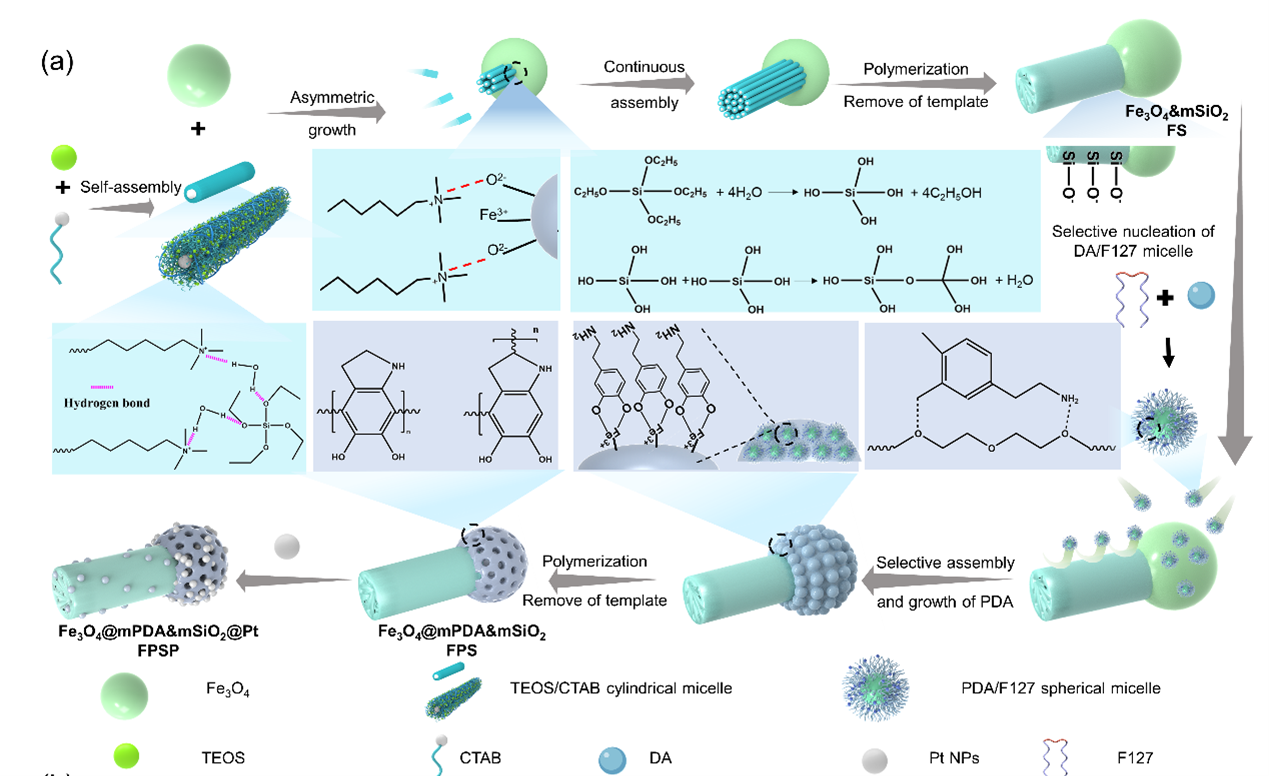
图1 纳米马达的合成路线图
在免疫检测应用中,团队以乳腺癌标志物CA153为模型,将自驱动纳米马达引入双抗体夹心免疫传感体系。红外光照诱导的自主运动显著提高了抗体标记与抗原分子的碰撞概率,使抗原捕获由“被动扩散”转向“主动寻靶”,捕获效率较静态标签提升95.8%。进一步地,纳米马达集成于夹心免疫传感器后实现了运动增强捕获与催化放大读出的协同,检测灵敏度较传统免疫传感器提升316.5倍,最低检测限达到0.0021 U·mL⁻¹,可在短时间内实现血清样本中CA153的高灵敏定量检测;该策略为早期肿瘤标志物检测以及环境监测等场景提供了更高效、更灵敏的免疫分析新方案。
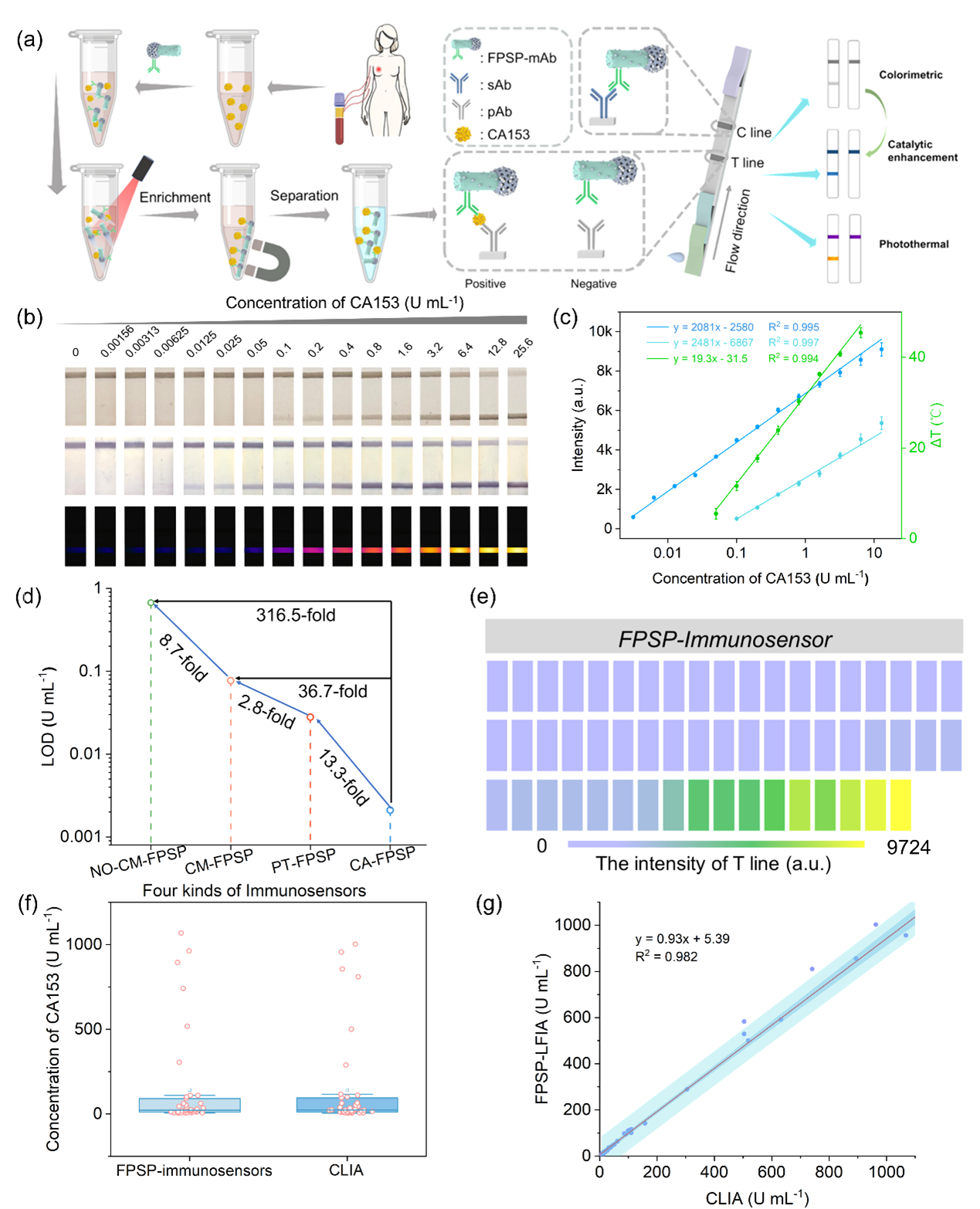
图2 基于纳米马达免疫传感器检测性能
文章信息
标题:Selective Interfacial Assembled Asymmetric Porous Nanomotors as Maneuverable Labels for Boosting Capture and Ultrasensitive Detection
期刊:Analytical Chemistry
链接:https://pubs.acs.org/doi/10.1021/acs.analchem.5c03501
BEBC理念
西安交通大学仿生工程与生物力学研究所(BEBC)围绕“重大疾病诊治”领域中共性科学问题和技术挑战,按照“临床重大需求牵引-生物力学理论创新-医工核心技术突破-临床转化应用推广”的研究思路,创立了“多尺度生物热-力-电耦合学”,开拓了“力-医学”学科新方向。BEBC立足力学基础理论,交叉融合材料、化学、生物、医学等领域,按照“临床问题(BED)-实验室研究(BENCH)-临床应用(BED)”的研究思路,在力学微环境领域开展了从组织到细胞和分子尺度的多尺度生物热-力-电耦合学等基础和应用研究,为阐明重大疾病的发病机理和临床诊疗提供有效的理论指导和技术方案。近年来,BEBC在生物力学和力学生物学的研究基础上,通过工程学手段,将不同尺度的力学调控引入疾病诊疗,开展了一系列的“力医学(mechanomedicine)”研究,在国内外权威期刊上系统阐释了力医学在不同疾病中的应用及前景。相关成果发表于《自然材料》(Nature Materials)、《自然化学》(Nature Chemistry)、《自然生物医学工程》(Nature Biomedical Engineering)、《自然通讯》(Nature Communications )、《科学进展》(Science Advances)、《美国科学院院报》(PNAS)等权威期刊。