近年来,外泌体作为干细胞治疗的“明星产品”,已成为再生医学领域的研究前沿和热点。大量研究表明,干细胞外泌体能够在创面愈合的各个阶段发挥作用,为治疗慢性难愈合创面这一临床难题带来新希望。然而,外泌体特征,生物学功能和递送效率受到细胞微环境中复杂的生化和生物物理因素影响,如何通过调控细胞微环境中理化因素来提高外泌体治疗效率是研究者面临的新挑战。
细胞微环境中理化因素对外泌体特征和生物学功能具有调控作用
外泌体是细胞通过旁分泌途径进行细胞间通讯的重要媒介。外泌体将核酸和蛋白质等内容物,运输进入靶细胞,能够引发靶细胞产生一系列生物反应,调节复杂的细胞内通路。细胞微环境中各种生化和生物物理因素对外泌体的产生、运输,特别是外泌体内容物的选择具有显著的调节作用(图1),这些调节作用可以被认为是细胞通过旁分泌途径,释放不同特性和功能的外泌体对微环境理化因素的适应作用。这一特性使得外泌体治疗能够被“设计”,因而在许多疾病治疗中显示出巨大潜力。目前,外泌体的设计策略在肿瘤和神经系统疾病的治疗中得到了迅速发展和广泛应用。大多数策略是增加外泌体在循环中的持续时间,并通过修饰表面蛋白优化外泌体靶向。然而,在慢性创面修复中,外泌体的远距离靶向释放并不是十分必要,而是需要不同的设计策略以提高外泌体在创面修复过程中的治疗效率。近日,西安交通大学生命学院仿生工程与生物力学研究所(BEBC)与空军军医大学第二附属医院烧伤整形科李靖主任团队合作,通过综述最新研究进展,创新性地提出:通过对细胞微环境中理化因素的干预可以调控外泌体的产量、递送效率和内容物,优化其在创面愈合过程中的特定生物学功能作为一种重要的设计策略。
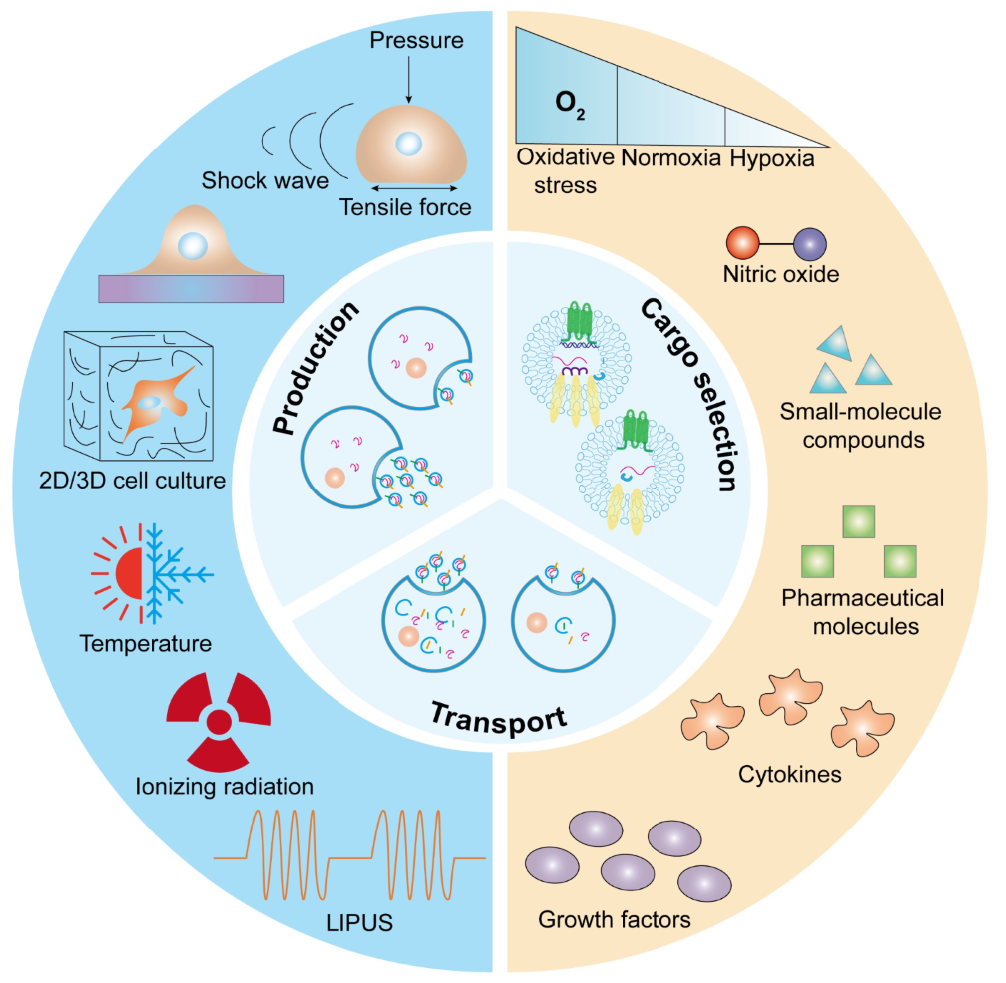
图1. 细胞微环境中生化和生物物理因素对外泌体特性的调控作用。
外泌体参与创面修复的多个过程,其促进慢性创面愈合的机制与调节复杂的细胞内信号通路相关
作为细胞旁分泌信号的载体,外泌体向靶细胞传递蛋白质、mRNAs、microRNAs和其他信号分子,通过调节不同的细胞内信号通路参与炎症调节、细胞增殖与迁移、血管新生、ECM重塑和抑制瘢痕形成等过程(图2),从而促进创面愈合,在慢性难愈合创面治疗中表现出巨大潜能。
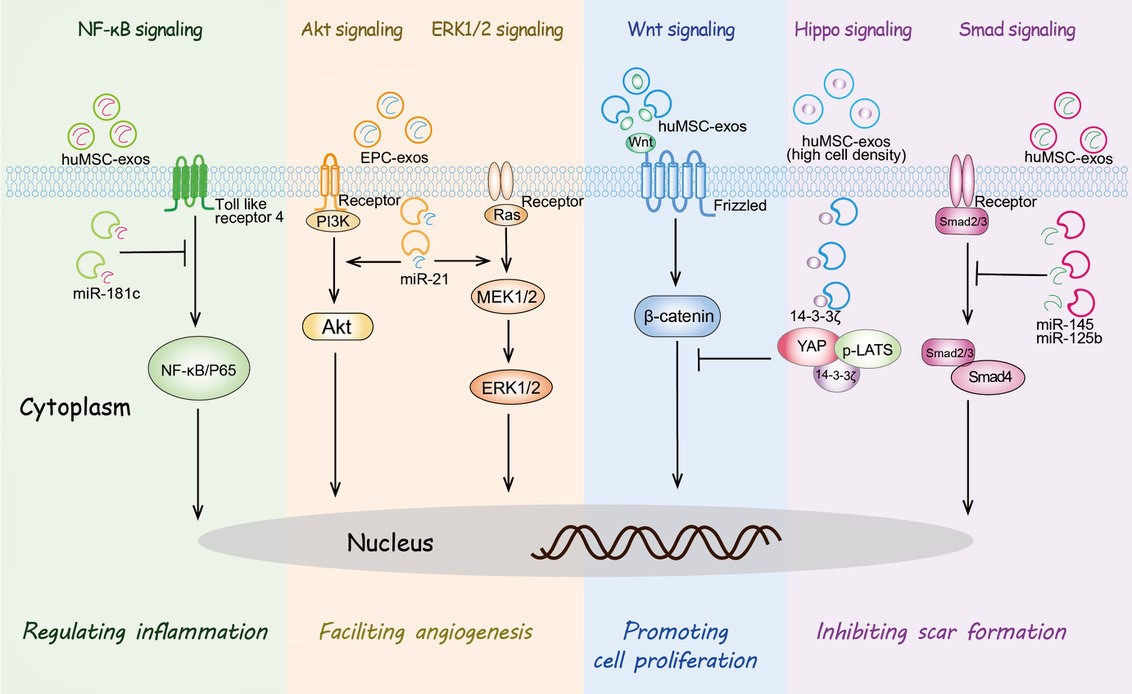
图2. 外泌体参与创面修复过程相关的信号通路调节。
基于水凝胶的递送系统可以储存并持续释放外泌体,为基于外泌体的慢性创面治疗带来极大可能
外泌体治疗的作用贯穿创面愈合的全过程。因此,如何持续有效地为创面提供外泌体是目前阻碍其应用的主要挑战。水凝胶具有与天然ECM相似的结构和性质,例如3D网状结构、良好的生物相容性和生物降解性等。因此许多研究通过水凝胶递送系统作为外泌体储存和持续释放的载体。将外泌体直接包裹在水凝胶中,或通过不同的物理/化学作用使外泌体与水凝胶结合,从而有效地提高外泌体在创面的释放效率(表1),为未来临床应用带来极大可能。
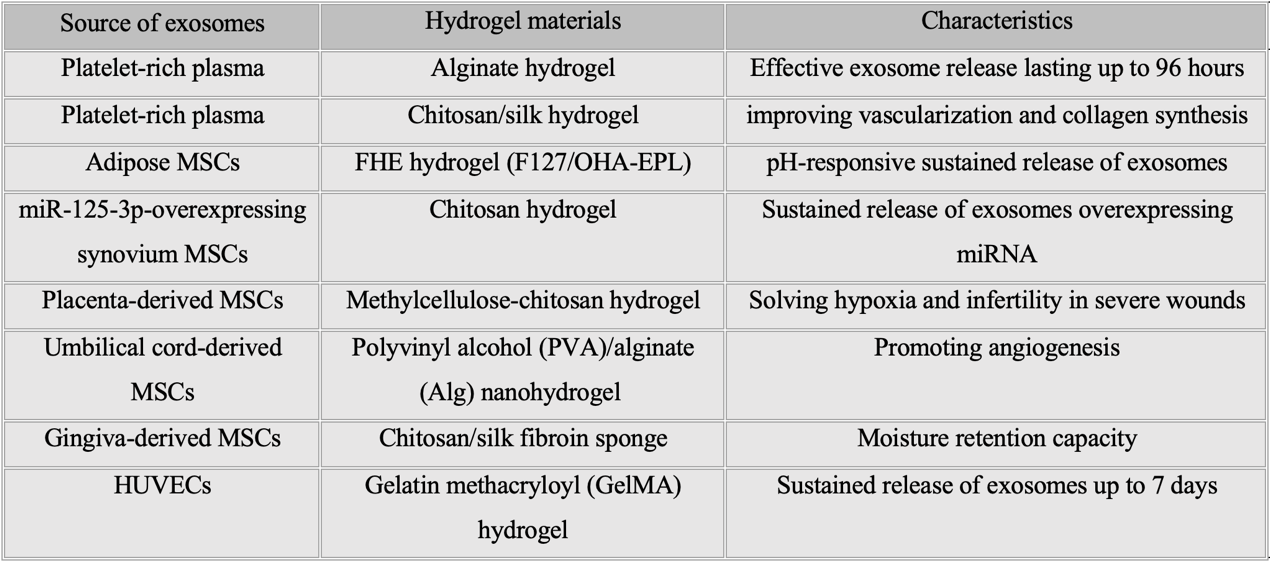
表1. 基于水凝胶材料的外泌体递送系统。
力证外泌体作为“无细胞的治疗技术”在组织修复领域的巨大潜力
近期,该文章发表在国际权威期刊NPG Asia Materials(DOI: 10.1038/s41427-022-00419-y),题目为“Microenvironmental Cue-Regulated Exosomes as Therapeutic Strategies for Improving Chronic Wound Healing”,并被选为NPG Asia Materials网页首页论文(图3)。空军军医大学第二附属医院烧伤整形科研究生戴炜作为第一作者,西安交通大学生命学院仿生工程与生物力学研究所(BEBC)马玉菲副教授和空军军医大学第二附属医院烧伤整形科李靖主任作为共同通讯作者。空军军医大学第二附属医院内分泌科高彬主任、西安交通大学第一附属医院肿瘤内科郭卉主任,西安交通大学生命学院BEBC徐峰教授为该文章的共同作者。文章不仅强调了外泌体作为“无细胞的治疗技术”在组织修复领域的巨大潜力,而且为今后深入研究细胞来源的外泌体治疗策略提出了新方向,为设计更有效的外泌体治疗策略提供了新思路。

图3. NPG Asia Materials网页首页论文。
原文链接:
https://www.nature.com/articles/s41427-022-00419-y