心血管疾病导致的心肌梗塞(MI)是全球范围内引起死亡的主要原因,在受损伤的心肌组织中会发生大量细胞(尤其是心肌细胞)的死亡,心室壁扩张,产生非收缩性瘢痕,最终形成心脏重塑并引起心力衰竭(HF)。在各种用于受损心肌组织再生的疗法中,基于干细胞的方法可以实现心肌细胞的再生,具有巨大的潜力。多项研究表明,静脉内注射或心肌内移植间充质干细胞(MSCs)均可减少梗塞心脏的纤维化面积并有效改善左心室功能,这一发现已经在多种MI动物模型中得到验证。然而,目前难以精确调控移植干细胞的命运,导致了细胞功能具有易变性,治疗结果较差。其中,移植后的干细胞向功能性心肌细胞分化的效率低下是阻碍心脏功能改善的主要原因之一。另外,用于心脏修复的干细胞疗法的机制仍不清楚,难以区分细胞移植后对心脏功能的改善是由分化、细胞间直接接触还是由旁分泌信号所介导。因此,指导移植后干细胞的分化和追踪干细胞在体内的行为对于揭示干细胞治疗机制和优化治疗效果至关重要。
针对这一难题,西安交通大学生命学院仿生工程与生物力学研究所(BEBC)的徐峰教授和靳国瑞副教授基于共轭聚合物纳米粒子开发了一种新型纳米平台(PFBT@miR-1-Tat NPs)。该平台可以实现miRNA-1在细胞内的触发释放,从而促进MSCs向心肌细胞的分化,并利用共轭聚合物PFBT稳定明亮的荧光实现对移植的MSCs的长期追踪,揭示了负载miR-1的MSCs修复受损心肌的机理。该工作中开发的共轭聚合物纳米载体将成为体内操纵移植细胞命运和揭示治疗机理的有力工具,这对于优化基因和细胞联合治疗的治疗方法至关重要,并因此加快临床转化的进程。相关研究以《Fluorescent Conjugated Polymer Nanovector for In Vivo Tracking and Regulating the Fate of Stem Cells for Restoring Infarcted Myocardium》为题发表在Acta Biomaterialia。
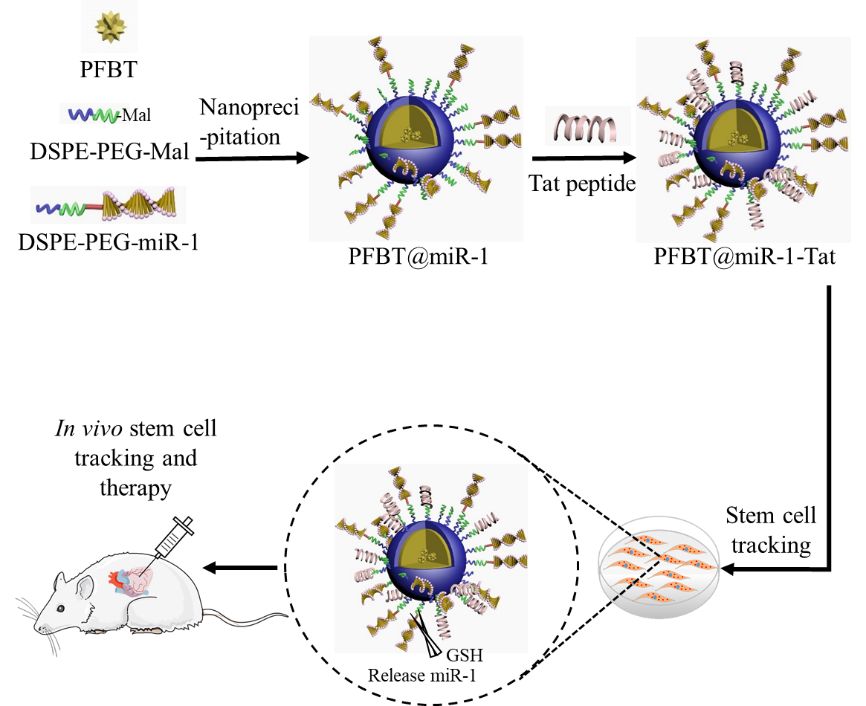
为了实现对心肌内移植干细胞命运的控制,研究者基于共轭聚合物纳米平台负载miR-1,通过基因的递送实现干细胞向心肌细胞的分化。在纳米平台构建之初,使用SPDP连接剂将miR-1与DSPE-PEG-NH2通过双硫键连接,该双硫键响应细胞内高浓度谷胱甘肽(GSH)发生断裂,实现miR-1的释放。体外研究表明,PFBT@miR-1-Tat NPs具有稳定的荧光特性,较高的基因释放效率,良好的生物相容性,高效的细胞转染效率和长期的细胞示踪能力,并促进了干细胞向心肌细胞的分化。转染了PFBT@miR-1-Tat NPs的干细胞进行心肌内移植后,在提高大鼠梗死心脏左心室射血分数(LVEF)和左心室短轴缩短分数(LVFS)以及减少心肌纤维化面积方面表现出卓越的能力。长期细胞追踪揭示治疗的主要机制是基因转染的干细胞可以实现向心肌细胞的分化,并与宿主心脏组织整合以恢复梗塞的心肌。而没有基因转染的干细胞主要通过旁分泌作用和血管形成来改善梗塞的心脏功能。研究表明,结合了细胞疗法和基因疗法的基因转染的干细胞可以实现心肌再生,对于从根本上治疗心力衰竭具有巨大的潜力。
BEBC靳国瑞副教授、研究生黎文芳和空军医科大学宋凡博士是本论文的共同第一作者,BEBC徐峰教授为通讯作者。西北大学赵婧博士、BEBC黄国友副教授及研究生王梦奇、刘倩对本研究做出了有益贡献。该研究获得了国家自然科学基金、陕西省自然科学基础研究计划、中国博士后科学基金资助项目和中央高校基础研究基金的支持。
BEBC通过理解和探索人体组织/细胞的微环境,将力学、化学、物理学与工程学、生物医学等领域进行交叉融合,通过“临床问题(BED)- 实验室研究(BENCH)- 临床应用(BED)”的研究策略,系统开展了细胞微环境的基础和应用研究,并将成果应用于药物筛选、疾病诊治和航天医学等生物医学领域。BEBC靳国瑞副教授课题组按照“细胞探针设计-体内验证-探针转化”的研究思路长期从事生多种细胞探针的开发及其在干细胞示踪揭示干细胞治疗机理及癌症诊疗中的应用研究。研究成果发表在Chemical Reviews, Chemical Society Reviews, Advanced Functional Materials, Biomaterials, Theranostics, Acta Biomaterialia, Chemical Communications, ACS Applied Materials & Interfaces, Nanoscale, Nanotechnology等学术期刊上。诚邀化学、材料、生物、医学、信息学专业的研究生、本科生及合作者,共同进行细胞示踪探针的开发和应用研究。
论文链接:https://www.sciencedirect.com/science/article/pii/S1742706120302075